Karcinom endometrijuma (KE) predstavlja najčešći malignitet ženskog reproduktivnog sistema u razvijenim zemljama, sa incidencijom koja raste paralelno sa starenjem populacije, prevalencijom gojaznosti i metaboličkim poremećajima. Njegova biološka osnova neraskidivo je povezana sa hormonskim disbalansom – pre svega produženom izloženošću estradiolu (E2) bez adekvatnog protivdejstva progesterona (P4). Ovaj disbalans direktno oblikuje imuni odgovor: dok E2 indukuje ekspresiju PD-L1 i olakšava imunološki beg tumora, P4 ispoljava protektivni efekat jačanjem antitumorskog imuniteta.
Uprkos decenijama stabilnog terapijskog pristupa zasnovanog na hirurgiji, radioterapiji i hemioterapiji, poslednjih godina dolazi do značajnog pomaka ka molekularno vođenom lečenju. U tom kontekstu, imunoterapija se pozicionira kao ključni novi pravac, naročito kod tumora sa poremećenim sistemom za popravku DNK (dMMR) i visokim mutacionim opterećenjem.
Međutim, klinički efekat imunoterapije nije uniforman. Odgovor na lečenje kritično zavisi od molekularnog podtipa, ali i od tumorskog mikrookruženja (TME). Faktori poput hipoksije i akumulacije laktata u TME dovode do terminalne iscrpljenosti T-ćelija, što limitira uspeh terapije čak i kod pacijenata sa povoljnim biomarkerima. Savremeni koncept lečenja se stoga pomera ka znatno kompleksnijem pitanju: u kom specifičnom biološkom kontekstu imunoterapija zaista im
Metodološki okvir i dizajn pregleda
Rad objavljen u Frontiers in Immunology predstavlja narativni pregled savremene literature sa ciljem integracije aktuelnih saznanja o ulozi imunoterapije u lečenju karcinoma endometrijuma. Poseban fokus stavljen je na mehaničku interakciju molekularnih, hormonskih i imunoloških faktora koji direktno oblikuju terapijski odgovor i diktiraju rezistenciju.
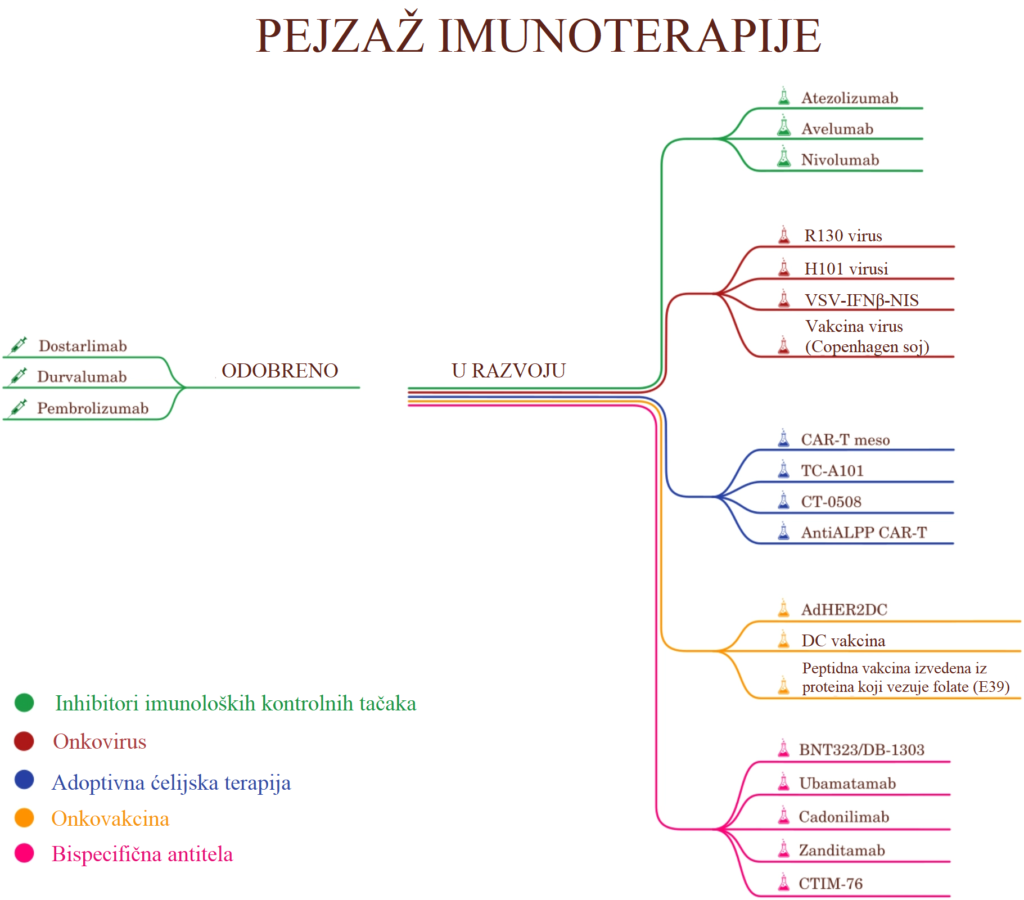
Autori sintetizuju podatke iz kliničkih studija različitih faza (uključujući ključne pivotalne studije inhibitora kontrolnih tačaka), translacionih istraživanja i molekularnih analiza. Pored etabliranih terapija, rad analizira i eksperimentalne pristupe u ranim fazama razvoja, kao što su antitumorske vakcine, onkolitički virusi i adoptivna ćelijska terapija (uključujući CAR-T pristupe), uz kritički osvrt na njihovu primenljivost u solidnim tumorima.
Analiza je strukturirana oko nekoliko ključnih osa:
- Savremena klasifikacija zasnovana na TCGA molekularnom profilisanju (POLEmut, dMMR, p53abn, p53wt);
- Uloga estradiola i progesterona u regulaciji imunološkog nadzora;
- Karakteristike tumorskog mikrookruženja (TME) kao barijere za efikasnost lekova;
- Klinička efikasnost i toksičnost postojećih imunoterapijskih strategija.
Kao pregledni rad, ovaj tekst ne donosi nove primarne podatke, već predstavlja interpretaciju postojećih dokaza. To podrazumeva inherentna ograničenja u pogledu heterogenosti uključenih studija i odsustva formalne meta-analitičke sinteze, ali nudi sveobuhvatan uvid u trenutne trendove koji menjaju kliničku praksu.
Savremeni terapijski pristup i mesto imunoterapije
Lečenje karcinoma endometrijuma i dalje se u najvećoj meri zasniva na klasičnim modalitetima, gde hirurgija (totalna histerektomija sa bilateralnom adneksektomijom) predstavlja osnovu terapije u ranim stadijumima. U zavisnosti od procene rizika, hirurški pristup se dopunjuje adjuvantnom radioterapijom i/ili hemioterapijom, pri čemu kombinacija karboplatina i paklitaksela ostaje standard u sistemskom lečenju uznapredovalih oblika bolesti.
Kod tumora sa očuvanom hormonskom zavisnošću primenjuje se i endokrina terapija (progestini, inhibitori aromataze), što reflektuje ulogu hormonskog disbalansa u progresiji bolesti. Međutim, ključni pomak ka molekularno vođenom lečenju donela je imunoterapija, čiji je položaj u terapijskom algoritmu sada jasno stratifikovan prema molekularnom profilu (POLEmut, dMMR, p53abn, p53wt).
Najizraženiji benefit inhibitora imunoloških kontrolnih tačaka (ICIs), poput pembrolizumaba i dostarlimaba, zabeležen je kod dMMR/MSI-H tumora. Studije poput RUBY i NRG-GY018 redefinisale su standard lečenja, pozicionirajući imunoterapiju u kombinaciji sa hemioterapijom već u prvoj liniji lečenja uznapredovale bolesti, što dovodi do značajnog produženja preživljavanja bez progresije (PFS).
| Terapijski režim | Brend naziv | Vrsta terapije | Indikacija FDA | Indikacija EMA |
|---|---|---|---|---|
| Pembrolizumab | Keytruda | Monoterapija | Uznapredovali, neresektabilni ili metastatski karcinom endometrijuma sa dMMR/MSI-H pozitivnim statusom, nakon progresije posle prethodnog sistemskog lečenja | Uznapredovali ili rekurentni karcinom endometrijuma sa dMMR/MSI-H pozitivnim statusom, sa progresijom tokom ili nakon prethodne terapije koja sadrži platinu, kod pacijentkinja koje nisu kandidati za kurativnu hirurgiju niti radioterapiju |
| Keytruda | U kombinaciji sa lenvatinibom | Uznapredovali karcinom endometrijuma sa dMMR/MSI-H negativnim statusom | Uznapredovali ili rekurentni karcinom endometrijuma sa progresijom tokom ili nakon prethodne terapije koja sadrži platinu, kod pacijentkinja koje nisu kandidati za kurativnu hirurgiju niti radioterapiju | |
| Keytruda | U kombinaciji sa hemioterapijom | Uznapredovali ili rekurentni karcinom endometrijuma | Prva linija lečenja primarno uznapredovalog ili rekurentnog karcinoma endometrijuma | |
| Durvalumab | Imfinzi | U kombinaciji sa hemioterapijom | Uznapredovali ili rekurentni karcinom endometrijuma sa dMMR pozitivnim statusom | Uznapredovali ili rekurentni karcinom endometrijuma za inicijalno lečenje; za terapiju održavanja kao monoterapija kod dMMR negativnog statusa i u kombinaciji sa olaparibom kod dMMR pozitivnog statusa |
| Dostarlimab-gxly | Jemperli | U kombinaciji sa hemioterapijom, nakon čega sledi dostarlimab kao monoterapija | Primarno uznapredovali ili rekurentni karcinom endometrijuma, sa ili bez dMMR/MSI-H statusa | Uznapredovali ili rekurentni karcinom endometrijuma pogodan za sistemsko lečenje |
Za pacijente sa pMMR/MSS statusom (koji čine većinu obolelih), monoterapija ICI najčešće ne pruža zadovoljavajući odgovor. U ovom kontekstu, studija Braszka et al. (2026) ističe važnost kombinovanih strategija, poput istovremene primene pembrolizumaba i lenvatiniba (multikinazni inhibitor), sa ciljem prevazilaženja primarne rezistencije i modifikacije imunosupresivnog mikrookruženja.
Mehanizmi rezistencije i personalizovana selekcija pacijenata
Iako imunoterapija predstavlja prekretnicu u lečenju karcinoma endometrijuma (KE), njen efekat je primarno ograničen na specifične molekularne podgrupe. Ograničena efikasnost kod većine pacijenata (naročito kod pMMR/MSS podtipa) proizlazi iz kompleksne interakcije između tumorskih ćelija, hormonskog miljea i visoko imunosupresivnog tumorskog mikrookruženja (TME).
U TME dominiraju inhibitorne ćelijske populacije, poput regulatornih T-limfocita (Tregs) i tumor-asociranih makrofaga (TAMs), koji u sinergiji sa metaboličkim faktorima – visokom koncentracijom laktata i hipoksijom – dovode do terminalne iscrpljenosti T-limfocita (T-cell exhaustion). Ovakve ćelije gube citotoksičnu moć i proliferativnu sposobnost, čineći ih imunološki „nemim“ na standardne inhibitore kontrolnih tačaka. Dodatni sloj rezistencije čine hormonski faktori: povišeni nivoi estradiola (E2) direktno indukuju ekspresiju PD-L1, dok gubitak protektivnog signaliziranja progesterona (P4) dodatno kompromituje imuni nadzor.
U svakodnevnoj kliničkoj praksi, odluka o primeni imunoterapije stoga ne sme biti uniformna, već integrisana u širi terapijski plan zasnovan na TCGA molekularnoj klasifikaciji:
- dMMR/MSI-H tumori: Zbog visokog mutacionog opterećenja i inherentne imunogenosti, ovi pacijenti su primarni kandidati za ranu primenu imunoterapije (često već u prvoj liniji uz hemioterapiju).
- pMMR/MSS tumori: Kod ove heterogene grupe, niska imunogenost zahteva primenu kombinovanih režima (npr. pembrolizumab + lenvatinib) kako bi se modifikovalo nepovoljno mikrookruženje i podstakao terapijski odgovor.
- p53-abnormalni (p53abn) tumori: Predstavljaju grupu visokog rizika gde se uloga imunoterapije intenzivno ispituje u okviru novih protokola (poput RAINBO platforme), s ciljem poboljšanja loše prognoze povezane sa ovim profilom.
Klinička vrednost imunoterapije, dakle, ne proizlazi samo iz puke identifikacije biomarkera, već iz sposobnosti da se molekularni profil integriše sa hormonskim i metaboličkim statusom pacijentkinje. Pravilna stratifikacija omogućava prelazak sa univerzalnog pristupa na precizno vođenu terapiju, birajući optimalni redosled lekova i kombinovane strategije tamo gde monoterapija nije dovoljna.
Perspektive razvoja i kliničke implikacije
Pored etabliranih inhibitora kontrolnih tačaka, istraživanja su usmerena ka prevazilaženju rezistencije putem inovativnih imunoterapijskih modaliteta. Iako su ovi pristupi još uvek u različitim fazama kliničkog ispitivanja, oni nagoveštavaju prelazak sa univerzalnih protokola na visoko specifične intervencije:
- Onkološke vakcine i onkolitički virusi: Fokusirani su na stimulaciju specifičnog imunog odgovora protiv tumorskih antigena i selektivnu onkolizu. Iako rani rezultati obećavaju, naročito u prevenciji recidiva, ključni izazov ostaje postizanje adekvatne jačine imunog odgovora u kompleksnom mikrookruženju solidnog tumora.
- Adoptivna ćelijska terapija (CAR-T) i bispecifična antitela: Ciljaju na direktno jačanje antitumorskog kapaciteta modifikovanih imunih ćelija. Međutim, njihova primena kod karcinoma endometrijuma (KE) suočava se sa barijerama poput hipoksije i metaboličke supresije (laktati) unutar TME.
Kliničke implikacije i personalizacija lečenja
Savremeni pristup lečenju karcinoma endometrijuma više se ne oslanja isključivo na stadijum bolesti, već na preciznu molekularnu stratifikaciju. Identifikacija podtipova, pre svega dMMR/MSI-H, ima direktan terapijski značaj i zahteva rano uvođenje imunoterapije. S druge strane, kompleksna interakcija hormonskog statusa i imunološkog odgovora otvara prostor za strategije koje kombinuju hormonsku terapiju i imunoterapiju, naročito kod tumora sa izraženom zavisnošću od estradiola.
U tom kontekstu, programi poput RAINBO (Refining Adjuvant Treatment In Endometrial Cancer Based On Molecular Profile) platforme predstavljaju budućnost kliničke prakse, jer integrišu molekularne biomarkere u dizajn adjuvantnih režima, čime se optimizuje balans između efikasnosti i toksičnosti.
Napomena:
Tekst predstavlja informativni prikaz objavljene naučne literature. Ne sadrži kliničke preporuke i ne može zameniti stručnu procenu lekara u realnim okolnostima. Pericardion nema finansijski niti komercijalni interes povezan sa temom ili sadržajem ovog teksta.