„Aktuelno lečenje adenokarcinoma pluća zasniva se na TNM sistemu stadijuma, koji obuhvata samo deo biološke heterogenosti bolesti i objašnjava manje od dve trećine prognostičkih varijabilnosti“, navode autori rada objavljenog u Journal of Clinical Oncology: Precision Oncology.
Ova konstatacija predstavlja osnovnu motivaciju studije.
Iako je stadijum I adenokarcinoma pluća definisan kao lokalizovana bolest, dugoročni ishodi nisu homogeni. Petogodišnje ukupno preživljavanje kreće se između 67% i 90%, uz rizik recidiva od približno 17,9%. Autori su želeli da utvrde da li se unutar istog TNM stadijuma mogu identifikovati biološki definisane podgrupe sa različitim rizikom i terapijskim implikacijama.
„Metaboličko reprogramiranje predstavlja jedno od temeljnih obeležja maligniteta“, podsećaju autori, ističući da prognostički modeli specifično razvijeni za stadijum I adenokarcinoma pluća do sada nisu postojali.
Sa tim ciljem konstruisan je metabolički uslovljen prognostički indeks (MAPI).
Analiza je obuhvatila 550 bolesnika sa stadijumom I adenokarcinoma pluća iz četiri nezavisne kohorte: TCGA kohorta (N=234) kao trening skup i tri validacione kohorte (GSE30219 N=78; GSE31210 N=168; FUSCC N=70), ukupno 316 bolesnika u validaciji.
Polazeći od 3.663 metabolička gena iz KEGG, REACTOME i Human-GEM baza, autori su primenom WGCNA analize, diferencijalne ekspresije i kombinacijama algoritama mašinskog učenja identifikovali 548 ključnih metaboličkih gena za konstrukciju modela. Kombinacija StepCox (forward) i Ridge algoritma pokazala je najviši C-indeks i izabrana je kao finalni MAPI model.
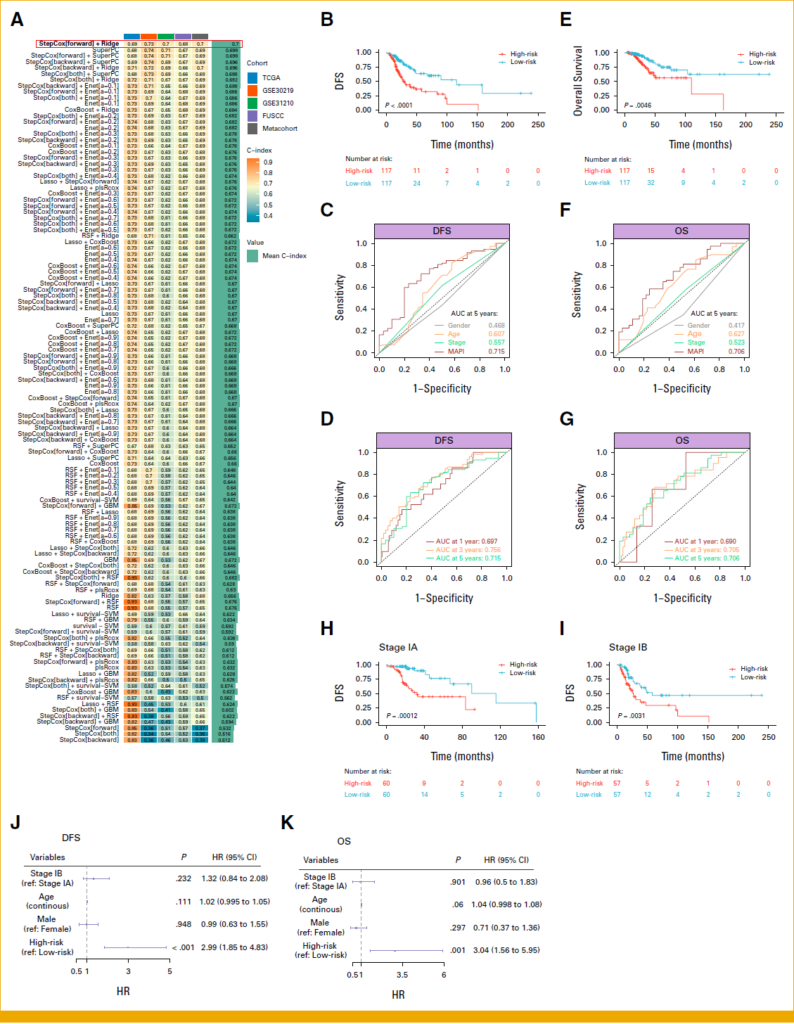
MAPI je robustno stratifikovao bolesnike u visokorizičnu i niskorizičnu grupu, sa statistički značajnim razlikama u preživljavanju bez znakova bolesti (DFS) i ukupnom preživljavanju (OS).
U validacionim kohortama, AUC vrednosti za 5-godišnje DFS dostizale su 0,772 (FUSCC kohorta), dok su za OS išle i do 0,803. U GSE30219 kohorti AUC za 1-godišnje DFS iznosio je 0,846. U ostalim analizama dugoročnih ishoda AUC vrednosti su se kretale približno između 0,73 i 0,80.
Multivarijantne Cox analize potvrdile su MAPI kao nezavisan prognostički faktor za DFS i OS.
Vizuelni prikaz konstrukcije modela, Kaplan–Meier krivih, ROC analiza i multivarijantnih modela prikazan je u Slici 1.
Autori su sigurni u vrednost svog rešenja: „Naši rezultati uspostavljaju MAPI kao biološki interpretabilan i klinički primenljiv alat za stratifikaciju rizika i donošenje odluka u preciznom lečenju bolesnika sa stadijumom I adenokarcinoma pluća.“
Razlike između MAPI grupa nisu zasnovane na samom postojanju metaboličkog reprogramiranja, već na različitim metaboličkim programima.
Visokorizična grupa bila je karakterisana:
- pojačanim metabolizmom glikana i kofaktora,
- višim tumorskim mutacionim opterećenjem (TMB),
- izraženijim svojstvima matičnih ćelija tumora (tzv. stemness),
- pojačanom proliferacijom i migracijom,
- fenotipom imunske isključenosti i nižom infiltracijom imunskih ćelija.
Nasuprot tome, niskorizična grupa pokazala je:
- pojačan lipidni metabolizam i metabolizam primarnih žučnih kiselina,
- izraženiju infiltraciju dendritskih ćelija, granulocita i limfocita,
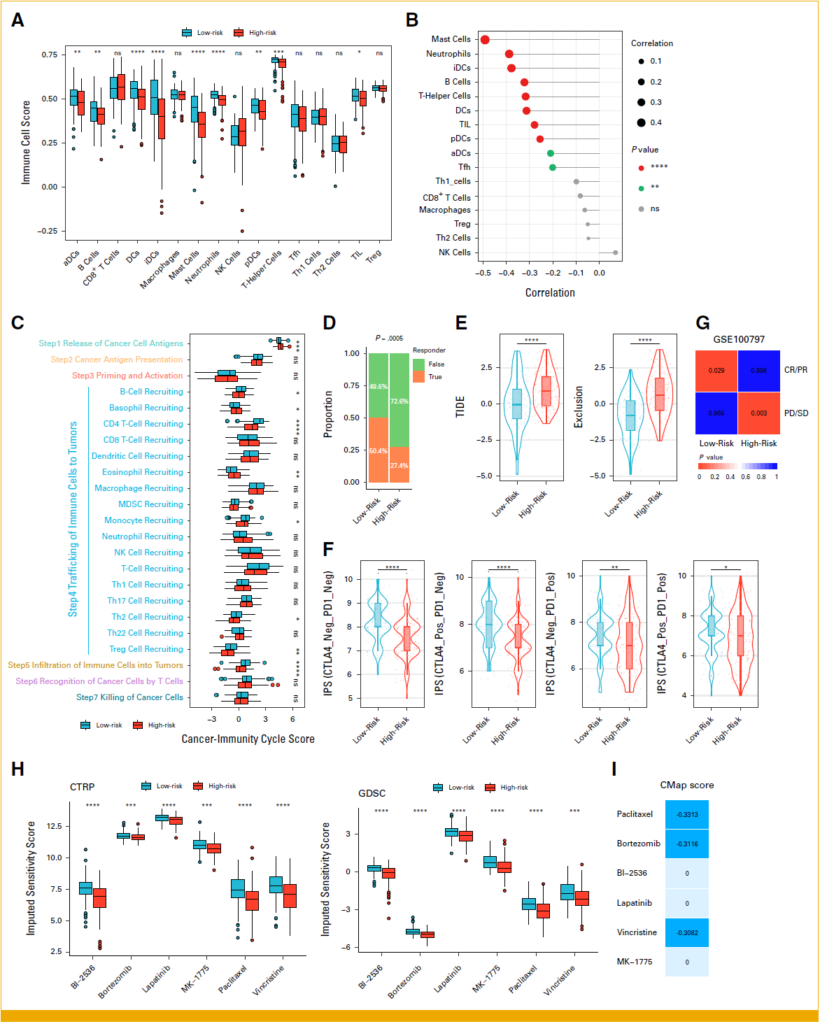
- niže TIDE skorove i niže skorove imunske isključenosti,
- viši IPS skor, što sugeriše potencijalni benefit od imunoterapije.
Na single-cell nivou (9 bolesnika: 3 adenokarcinoma in situ, 3 minimalno invazivna adenokarcinoma i 3 invazivna adenokarcinoma), MAPI skor bio je viši u invazivnim lezijama i pozitivno je korelirao sa indeksom nediferenciranosti (CytoTRACE), što dodatno potvrđuje povezanost ovog indeksa sa progresijom bolesti. Ovi nalazi sugerišu da MAPI ne predstavlja samo statistički konstrukt, već odražava dublje biološke karakteristike tumora. U skladu sa tim, detaljna analiza tumorskog mikrookruženja pokazala je da je niskorizična grupa imunološki aktivnija, sa pojačanom infiltracijom imunskih ćelija i izraženijom aktivnošću faza ciklusa antitumorskog imuniteta, dok je u visokorizičnoj grupi dominirao obrazac imunske isključenosti.
S obzirom na predikovani slabiji odgovor na imunoterapiju u visokorizičnoj grupi, autori su sproveli farmakogenomsku analizu, koja je inicijalno identifikovala šest potencijalnih jedinjenja (BI-2536, bortezomib, lapatinib, MK-1775, paklitaksel i vinkristin). Među njima su paklitaksel, bortezomib i vinkristin imali CMap skor manji od 0, što sugeriše potencijal da delimično preokrenu transkripcioni program visokog rizika ka transkripcionom profilu niskog rizika ili normalnog tkiva. Ovi nalazi, zajedno sa analizama TIDE i IPS skorova, prikazani su na Slici 2.
Autori naglašavaju da su terapijske implikacije zasnovane na in silico analizama i da predstavljaju hipoteza-generišuće nalaze koji zahtevaju dalju funkcionalnu i kliničku validaciju. Za razliku od čisto matematičkih prognostičkih potpisa, MAPI uključuje gene sa potvrđenom funkcionalnom ulogom. DEGS1 i PLOD1, koji najviše doprinose MAPI skoru, povezani su sa lošijim preživljavanjem bez znakova bolesti, a njihova supresija u in vitro eksperimentima značajno je smanjila proliferaciju i migraciju ćelija adenokarcinoma pluća. Time model dobija biološko objašnjenje svojih prognostičkih rezultata, za razliku od modela koji funkcionišu isključivo kao statistički algoritmi bez jasne biološke podloge.
Što se organičenja studije koju su autori naveli tiče, ona je retrospektivna, a broj bolesnika u single-cell validaciji bio je ograničen (N=9). Analiza osetljivosti na lekove sprovedena je in silico i zahteva prospektivnu kliničku potvrdu. Takođe, model nije validiran primenom nested cross-validation pristupa.
Autori eksplicitno navode potrebu za daljom prospektivnom validacijom pre eventualne kliničke primene.
“Ovaj rad pokazuje da metabolički genski potpis može robustno stratifikovati rizik u stadijumu I adenokarcinoma pluća i povezati molekularne karakteristike tumora sa kliničkim ishodom” – navodi se u zaključku studije. “Integracijom metabolizma, genetskih alteracija, imunoloških karakteristika i funkcionalne validacije, MAPI predstavlja pokušaj da se biološka heterogenost rane bolesti preciznije definiše i potencijalno iskoristi u okviru precizne onkologije.“
Link na originalni članak možete pronaći ovde.
Napomena: Tekst predstavlja informativni prikaz objavljene naučne literature. Ne sadrži kliničke preporuke i ne može zameniti stručnu procenu lekara u realnim okolnostima.