Produženje intervala između doza rituksimaba sa šest na dvanaest meseci kod osoba sa relapsnim tokom multiple skleroze (RMS) nije bilo povezano sa statistički značajnim povećanjem rizika od ponovne aktivnosti bolesti tokom praćenja do četiri godine. Iako studija koju predstavljamo koristi termin RMS, pacijenti sa sekundarno progresivnom multiplom sklerozom (SPMS) su bili isključeni, pa analizirana populacija praktično odgovara osobama sa relapsno-remitentnom formom bolesti (RRMS). Svi uključeni pacijenti imali su prethodno visoko aktivnu bolest, definisanu relapsom u prethodne dve godine i/ili prisustvom MRI aktivnosti u prethodnoj godini.
Analiza, objavljena u časopisu Neurology, zasnovana je na emulaciji randomizovanog kontrolisanog ispitivanja („target trial“) i obuhvatila je pacijente koji su tokom prve godine terapije rituksimabom postigli status bez dokaza o aktivnosti bolesti (NEDA‑3). Početak praćenja (“baseline”) definisan je kao ulazak u drugu godinu terapije. NEDA‑3 je podrazumevao odsustvo kliničkih relapsa, odsustvo nove ili uvećane MRI lezije i odsustvo potvrđene progresije invaliditeta prema EDSS kriterijumima (povećanje od 0,5 do 1,5 poena u zavisnosti od početnog EDSS skora).
Tabela 1. Kliničke i demografske karakteristike osoba u emulaciji ciljanog ispitivanja
| RTX 500 mg na 12 meseci (n = 140) | RTX 500 mg na 6 meseci (n = 468) | |
|---|---|---|
| Karakteristike na početku (baseline) | ||
| Starost, godine, srednja vrednost (SD) | 40.4 (11.0) | 38.4 (9.9) |
| Ženski pol, n (%) | 103 (73.6) | 332 (70.9) |
| Rasa i etnička pripadnost, n (%) | ||
| Azijati/Pacifička ostrva | 7 (5.0) | 9 (1.9) |
| Crna rasa | 19 (13.6) | 71 (15.2) |
| Hispano/latino | 54 (38.6) | 173 (37.0) |
| Mešovito | 0 (0) | 1 (0.2) |
| Bela rasa | 60 (42.9) | 214 (45.7) |
| BMI | ||
| Medijana (IQR) | 29.3 (26.1–36.2) | 28.5 (24.5–34.7) |
| Gojazni (BMI ≥30), n (%) | 67 (47.9) | 197 (42.1) |
| Trajanje bolesti, godine, medijana (IQR) | 4.3 (1.7–10.3) | 5.6 (2.5–11.3) |
| EDSS, medijana (IQR) | 1.5 (1.0–2.0) | 2.0 (1.0–2.25) |
| Poboljšanje invaliditeta tokom prve godine na RTX, n (%) | 44 (31.4) | 133 (28.4) |
| Kumulativna doza RTX, mg, medijana (IQR) | 1.500 (1.000–1.500) | 1.500 (1.500–2.000) |
| Karakteristike pri započinjanju RTX | ||
| Aktivnost bolesti, n (%) | ||
| Relaps u prethodne 2 godine | 112 (80.0) | 387 (82.7) |
| MRI aktivnost u prethodnoj godini | 105 (75.0) | 382 (81.6) |
| Relaps i/ili MRI aktivnost | 140 (100) | 486 (100) |
| Godišnja stopa relapsa u prethodnoj godini (95% CI) | 0.90 (0.73–1.08) | 0.88 (0.79–0.97) |
| EDSS, medijana (IQR) | 2.0 (1.0–2.5) | 2.0 (1.5–3.0) |
| Prethodna DMT terapija, n (%) | ||
| Bez terapije | 79 (56.4) | 183 (39.1) |
| Visoko efikasna terapija (HET) | 12 (8.6) | 59 (12.6) |
| Umereno efikasna terapija (meDMT) | 49 (35.0) | 226 (48.3) |
| Godina započinjanja RTX, medijana (IQR) | 2019 (2018.5–2020) | 2018 (2017–2019) |
U poređenju dve strategije održavanja – rituksimab 500 mg na svakih šest meseci naspram 500 mg na svakih 12 meseci – istraživači su analizirali visoko selektovanu populaciju sa stabilnom bolešću tokom prve godine terapije. Važno je napomenuti da je grupa koja je kasnije prešla na godišnje doziranje imala nižu kumulativnu dozu rituksimaba već tokom prve godine (medijana 1000–1500 mg), u poređenju sa q6mo grupom (1500–2000 mg), što je relevantno u kontekstu rizika od infekcija.
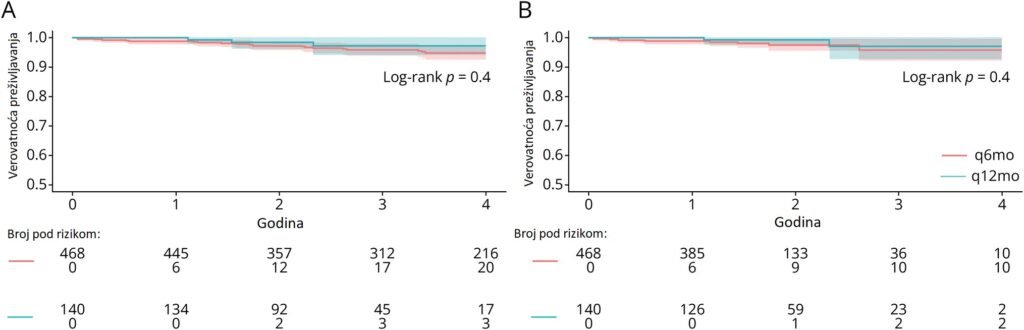
Ova slika prikazuje Kaplan–Meier krive koje prikazuju verovatnoću gubitka NEDA-3 (relaps, MRI aktivnost bolesti i/ili progresija invaliditeta, NEDA-3) kod osoba sa relapsnim tokom multiple skleroze (pwRMS) lečenih rituksimabom 500 mg na svakih 12 meseci (linija u akva boji) i na svakih 6 meseci (crvena linija), nakon jedne godine postignutog NEDA-3 na rituksimabu. Panel A prikazuje rezultate analiza po principu intention-to-treat, a panel B analiza po protokolu (per-protocol). Ukupan rizik gubitka NEDA-3 bio je nizak u obe grupe i nije bilo statistički značajne razlike između grupa tokom prve 4 godine praćenja, ni u intention-to-treat ni u per-protocol analizama.
Skraćenice:
NEDA-3 = bez dokaza o aktivnosti bolesti-3;
pwRMS = osobe sa relapsnim tokom multiple skleroze;
q6mo = na svakih 6 meseci;
q12mo = na svakih 12 meseci.
Produženje intervala između doza nije bilo povezano sa statistički značajnim povećanjem rizika od relapsa, nove MRI aktivnosti ili gubitka NEDA‑3 statusa. U primarnom, propensity score‑adjusted ITT modelu, rizik gubitka NEDA‑3 nije bio statistički značajno različit između strategija (HR 1,60; 95% CI 0,69–3,68), uz slične rezultate u per‑protocol analizi (HR 1,44; 95% CI 0,45–4,61). Ukupan broj događaja bio je nizak, što ograničava preciznost procene razlika.
Tabela 2. Ishodi
| RTX 500 mg na 12 meseci (n = 140) | RTX 500 mg na 6 meseci (n = 468) | |
|---|---|---|
| Gubitak NEDA-3 statusa | ||
| Populacija predviđena za lečenje (ITT) | ||
| n (%) | 3 (2.14) | 20 (4.27) |
| HR (95% CI), p vrednost, IPTW | 1.41 (0.62–3.21), 0.4140 | Referenca |
| Dodatno prilagođeno za kontrolne MRI preglede mozga | 1.20 (0.52–2.74), 0.6683 | Referenca |
| Per-protocol | ||
| n (%) | 2 (1.43) | 10 (2.14) |
| HR (95% CI), p vrednost, IPTW | 1.17 (0.37–3.65), 0.7918 | Referenca |
| Dodatno prilagođeno za kontrolne MRI preglede mozga | 1.06 (0.34–3.32), 0.9206 | Referenca |
| Relaps i/ili MRI aktivnost bolesti | ||
| Populacija predviđena za lečenje (ITT) | ||
| n (%) | 3 (2.14) | 18 (3.85) |
| HR (95% CI), p vrednost, IPTW | 1.54 (0.67–3.56), 0.3097 | Referenca |
| Dodatno prilagođeno za kontrolne MRI preglede mozga | 1.45 (0.63–3.35), 0.3887 | Referenca |
| Per-protocol | ||
| n (%) | 2 (1.43) | 10 (2.14) |
| HR (95% CI), p vrednost, IPTW | 1.17 (0.37–3.65), 0.7918 | Referenca |
| Dodatno prilagođeno za kontrolne MRI preglede mozga | 1.06 (0.34–3.32), 0.9206 | Referenca |
| Relapsi | ||
| Populacija predviđena za lečenje (ITT) | ||
| n (%) | 2 (1.43) | 11 (2.35) |
| Osoba-godine | 361.66 | 1,477.19 |
| Stopa/100 osoba-godina (95% CI) | 0.55 (−0.21–1.32) | 0.75 (0.31–1.19) |
| Per-protocol | ||
| n (%) | 1 (0.71) | 6 (1.28) |
| Osoba-godine | 283.79 | 767.78 |
| Stopa/100 osoba-godina (95% CI) | 0.35 (−0.34–1.04) | 0.78 (0.16–1.41) |
| Progresija invaliditeta | ||
| Populacija predviđena za lečenje (ITT), n (%) | 1 (0.71) | 4 (0.85) |
| Per-protocol, n (%) | 0 | 0 |
Iako je broj perifernih B‑ćelija bio sličan između grupa na početku, tokom praćenja je značajno češće dolazilo do repopulacije B‑ćelija u grupi sa godišnjim doziranjem. Repopulacija ≥80 ćelija/μL zabeležena je kod 75,7% pacijenata u q12mo grupi, u poređenju sa 60,2% u q6mo grupi (ITT analiza). Uprkos tome, u ovoj kohorti porast broja B‑ćelija nije bio povezan sa povećanim rizikom od kliničkih relapsa ili nove MRI aktivnosti, što sugeriše da kontinuirana deplecija B‑ćelija možda nije neophodna za održavanje kontrole bolesti kod pažljivo odabrane populacije sa stabilnom RMS.
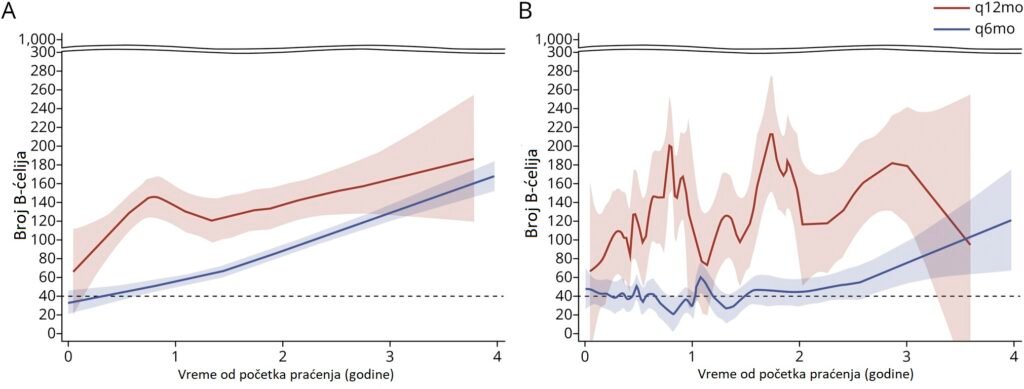
Prikazane su prosečne apsolutne vrednosti CD19+ B-ćelija po mikrolitru (μL) kod osoba lečenih rituksimabom 500 mg na svakih 12 meseci (crvena linija) nakon prve godine terapije rituksimabom i kod onih lečenih na svakih 6 meseci (plava linija). Osenčene oblasti predstavljaju 95% intervale poverenja. Panel A prikazuje rezultate analiza po principu intention-to-treat, a panel B rezultate analiza po protokolu (per-protocol). Vreme nula (baseline) definisano je kao početak druge godine nakon prve infuzije rituksimaba.
Vrednosti B-ćelija na početku praćenja nisu se značajno razlikovale između grupa, što ukazuje da niske vrednosti B-ćelija nisu bile glavni faktor u odluci o produženju intervala doziranja. Očekivano, broj B-ćelija se povećavao nakon produženja intervala doziranja u q12mo grupi, pri čemu je većina ispitanika u obe analize imala vrednosti iznad 80 ćelija/μL.
U per-protocol analizama, q6mo grupa je održavala značajno niže vrednosti B-ćelija u poređenju sa q12mo grupom, pri čemu je samo 23,3% ispitanika imalo vrednosti B-ćelija ≥80 ćelija/μL barem jednom tokom praćenja. U intention-to-treat analizama, gde je 66,9% ispitanika u q6mo grupi prešlo na niže doze ili produžene intervale, vrednosti B-ćelija su porasle i u q6mo grupi.
Vrednosti iznad 300 ćelija/μL nisu prikazane. Samo 4 ispitanika nisu imali dostupna merenja B-ćelija tokom perioda praćenja.
Skraćenice:
q6mo = na svakih 6 meseci;
q12mo = na svakih 12 meseci.
Zaključak:
Produženje intervala između doza rituksimaba na 12 meseci, nakon najmanje jedne godine stabilnosti bolesti (NEDA-3), nije bilo povezano sa statistički značajnim povećanjem rizika od aktivnosti bolesti u poređenju sa standardnim šestomesečnim režimom tokom praćenja do četiri godine. Stabilnost bolesti održana je kod više od 95% ispitanika u obe grupe.
Tumačenje ovih nalaza zahteva oprez. Tokom praćenja deo ispitanika menjao je režim doziranja, što odražava realnu kliničku praksu, ali ograničava mogućnost striktne komparacije strategija. Opservacioni dizajn, uprkos primeni metode emulacije randomizovanog ispitivanja, ne isključuje uticaj faktora koji nisu u potpunosti kontrolisani i koji mogu uticati na razlike između grupa. Dodatno, mali broj događaja ograničava preciznost procene tih razlika. Praćenje do četiri godine nije dovoljno za procenu dugoročnih ishoda, uključujući akumulaciju invaliditeta.
U tom kontekstu, ovi nalazi predstavljaju dokaze klase IV i ukazuju da produženje intervala doziranja može biti razmatrano kod pažljivo odabranih pacijenata sa stabilnom bolešću, uz oprez u interpretaciji.
Napomena:
Tekst predstavlja informativni prikaz objavljene naučne literature. Ne sadrži kliničke preporuke i ne može zameniti stručnu procenu lekara u realnim okolnostima. Pericardion nema finansijski niti komercijalni interes povezan sa temom ili sadržajem ovog teksta.