Standardne CAR-T ćelije u solidnim tumorima gube TCF1⁺ „stem-like“ rezervoar zbog MHC-nezavisnog prepoznavanja antigena i ranog epigenetskog utišavanja Tcf7 lokusa.
Genetska modifikacija CAR-T ćelija overekspresijom c-Jun transkripcionog faktora sprečava epigenetski „lockdown“ i omogućava formiranje vitalne progenitorske baze direktno u tumoru.
Studija otkriva da PD-1 signalizacija aktivno destabilizuje c-Jun protein, putem inhibicije MAPK/PI3K signalnih puteva, gurajući ga u proteozomsku degradaciju.
Blokada PD-L1 „spasava“ c-Jun protein od degradacije. Kombinacija c-Jun modifikacije i anti-PD-L1 terapije dovodi do desetostrukog povećanja infiltracije i skoro potpune eliminacije agresivnih tumora.
Modifikovane CAR-T ćelije deluju kao katalizator menjajući tumorsko mikrookruženje i uspešno regrutujući endogene CD8⁺ T ćelije domaćina u antitumorski odgovor.
Svi znamo klasičnu priču: CAR-T ćelije su napravile revoluciju u hematologiji, ali čim zakorače na „neprijateljsku teritoriju“ solidnih tumora (poput NSCLC ili TNBC), stvari postaju komplikovane. U radu objavljenom u Science Immunology, Snyder i saradnici postavljaju suštinsko pitanje: Zašto ove „super-ćelije“ tako brzo ostaju bez goriva?
Fokus istraživanja je na populaciji PD-1⁺TCF1⁺ „stem-like“ T ćelija. One funkcionišu kao unutrašnji rezervoar – ako nema ovih ćelija, nema ni novih efektorskih „regruta“, a antitumorski odgovor se gasi pre nego što je praktično i počeo.
Zanimljivost: MHC-nezavisnost kao „Ahilova peta“
Ovde dolazimo do fascinantnog paradoksa. Dok prirodne T ćelije prolaze kroz „edukaciju“ kod dendritičnih ćelija u limfnim čvorovima (gde im MHC-zavisni signali pomažu da zadrže taj dragoceni „stem-like“ status), CAR-T ćelije su „slobodni strelci“. One prepoznaju antigen direktno, nezavisno od MHC molekula.
U čemu je problem? Upravo ta nezavisnost postaje njihova slaba tačka. Preskačući zaštitne niše u limfnim čvorovima, CAR-T ćelije jure direktno u „osinje gnezdo“ tumora. Tamo su odmah izložene surovim uslovima mikrookruženja koji ih guraju u ekspresnu terminalnu iscrpljenost, bez mehanizma za obnovu sopstvenih snaga.
MHC-nezavisnost kao „Ahilova peta“
Ovde dolazimo do fascinantnog paradoksa. Dok prirodne T ćelije prolaze kroz „edukaciju“ kod dendritičnih ćelija u limfnim čvorovima, gde im MHC-zavisni signali pomažu da zadrže dragoceni „stem-like“ status, CAR-T ćelije funkcionišu kao svojevrsni „slobodni strelci“. One prepoznaju antigen direktno, nezavisno od MHC molekula.
U čemu je problem? Upravo ta nezavisnost postaje njihova slaba tačka. Preskačući zaštitne niše u limfnim čvorovima, CAR-T ćelije jure pravo u „osinje gnezdo“ tumora. Tamo su odmah izložene surovim uslovima tumorskog mikrookruženja koji ih guraju u ekspresnu terminalnu iscrpljenost, bez mehanizma za obnovu sopstvenih snaga.
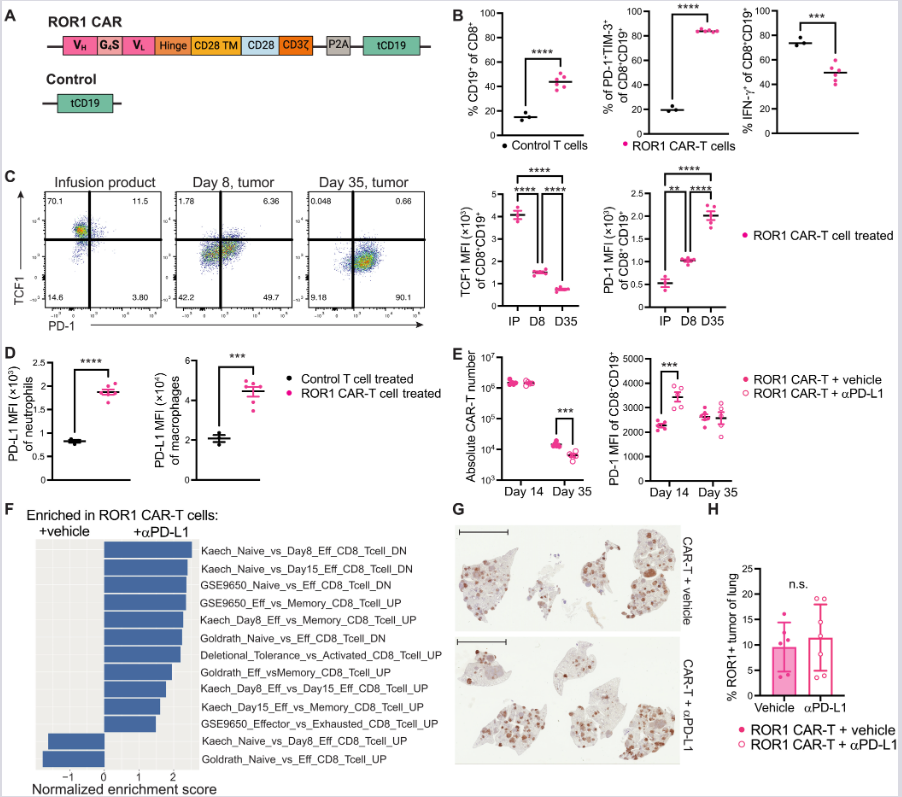
(A–C) Retrovirusni konstrukt (A) i fenotipska analiza CD8⁺ CAR-T ćelija 8. dana nakon infuzije (B, C). Flow citometrija potvrđuje visoku ekspresiju PD-1/TIM-3 i progresivni gubitak TCF1 u tumorskom tkivu. n = 3–6 miševa/grupi.
(D–F) Ekspresija PD-L1 na mijeloidnim ćelijama (D) i efekat anti-PD-L1 terapije na broj i fenotip CAR-T ćelija (E). GSEA analiza (F) pokazuje odsustvo značajnog transkripcionog odgovora na blokadu PD-L1 kod standardnih CAR-T ćelija. n = 3–6 miševa/grupi.
(G, H) Reprezentativna IHC analiza ROR1⁺ tumora u plućima 45. dana. Kvantifikacija (H) potvrđuje izostanak terapijskog efekta anti-PD-L1 antitela na progresiju bolesti. n = 6–7 miševa/grupi. Skala: 5 mm.
Statistička analiza: (B, D, E, H) neupareni dvostrani t-test, (C) jednofaktorska ANOVA (Tukey-jev test). Rezultati dva nezavisna eksperimenta.
*P < 0,01; **P < 0,001; ***P < 0,0001.
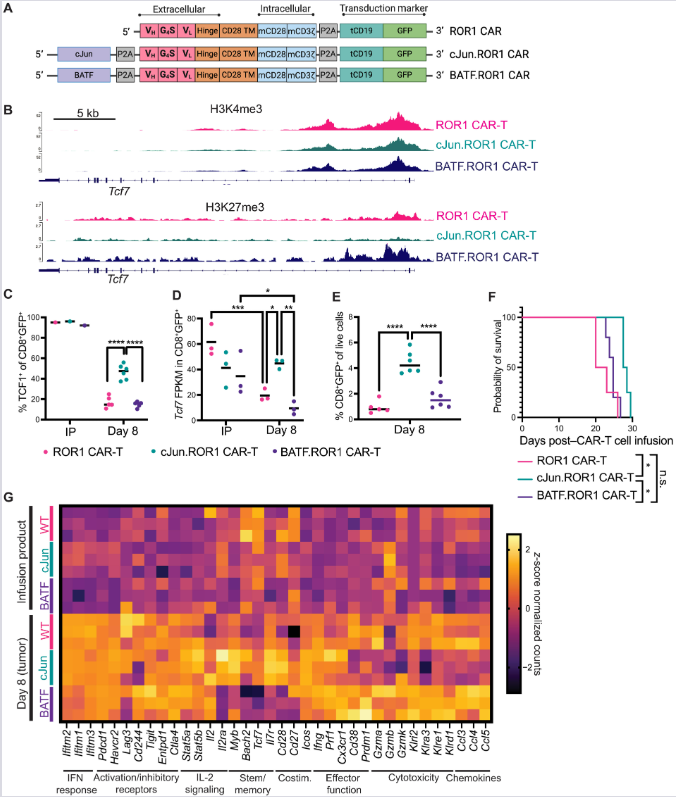
(A, B) Retrovirusni konstrukti i prikaz u pretraživaču genoma (genome-browser) za histonske modifikacije (H3K4me3 i H3K27me3) na Tcf7 lokusu u CAR-T infuzionim proizvodima (IP).
(C, D) Nivo TCF1 proteina (C) i transkripta Tcf7 (D) u infuzionom proizvodu i tumorskom tkivu 8. dana. c-Jun održava TCF1, dok ga BATF dodatno smanjuje. n = 3–6 miševa/grupi.
(E, F) Akumulacija CAR-T ćelija u tumoru (E) i preživljavanje miševa (F) nakon Cy + CAR-T terapije. cJun.ROR1 varijanta pokazuje superiornu akumulaciju i preživljavanje. n = 4–6 miševa/grupi.
(G) Toplotna mapa (heatmap) z-score normalizovane ekspresije probranih gena u IP i tumoru 8. dana. n = 3 miša/grupi.
Statistička analiza: (C, D) dvofaktorska ANOVA, (E) jednofaktorska ANOVA (Tukey-jev test), (F) log-rank Mantel–Cox test. Rezultati dva nezavisna eksperimenta.
*P < 0,05; **P < 0,01; ***P < 0,001; ****P < 0,0001.
Epigenetski „lockdown“: Zašto Tcf7 gen ide pod katanac?
Pre same infuzije, CAR-T ćelije u laboratoriji izgledaju optimalno – karakteriše ih visoka ekspresija transkripcionog faktora TCF1, ključnog čuvara njihovog „stem-like“ karaktera. Međutim, čim prodru u tumorsko mikrookruženje, situacija se drastično menja. Autori su dokumentovali ubrzan pad TCF1 ekspresije, pri čemu ćelije poprimaju nepovoljan fenotip:
- Nagla pojava inhibitornog receptora PD-1.
- Gubitak TCF1.
- Akumulacija markera terminalne iscrpljenosti, poput TIM-3.
Šta se dešava u „mašinskoj sobi“ ćelije?
Nije reč o običnom umoru, već o dubokom epigenetskom remodelingu. Gen Tcf7 (koji kodira TCF1) biva bukvalno zaključan progresijom represivnih histonskih modifikacija. Konkretno, reč je o H3K27me3 markerima. Ovo nije samo prolazna iscrpljenost, već sistemski, epigenetski „lockdown“. On pretvara CAR-T ćeliju u terminalno iscrpljenog vojnika bez kapaciteta za samorenovaciju. Bez TCF1, „stem-like“ rezervoar nepovratno presušuje.
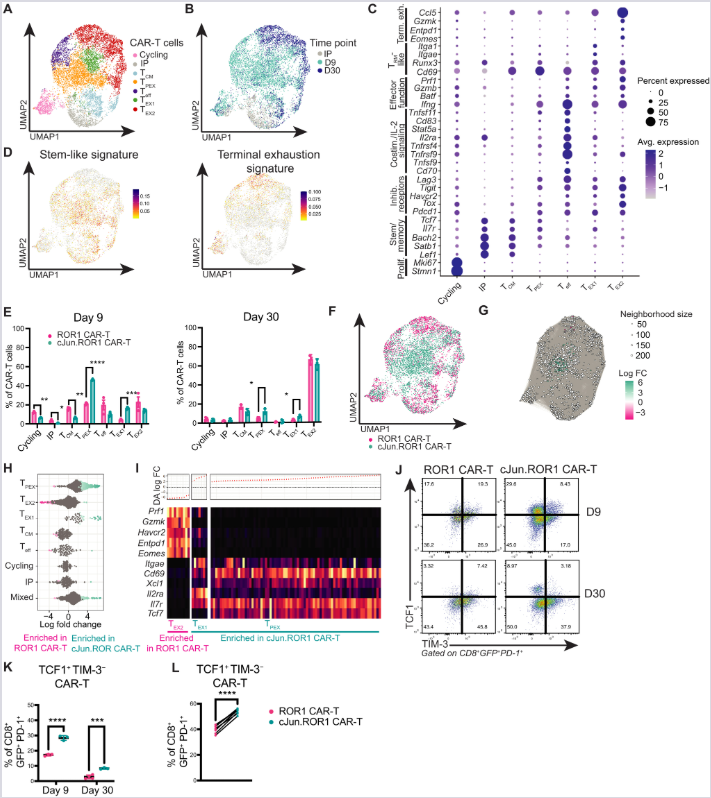
(A–C) scRNA-seq analiza i nenadzirano klasterovanje cJun.ROR1 i standardnih CAR-T ćelija (IP, dan 9 i 30 post-infuzije). Dot-plot (C) identifikuje ključne genske potpise subklastera.
(D–F) Skorovi obogaćenja signalnih puteva (D) i distribucija cJun.ROR1 vs. ROR1 ćelija po klasterima (E, F). n = 3 miša/grupi.
(G–I) Analiza mikrosusedstava (k-NN graf): diferencijalna zastupljenost (DA log₂ FC > 3) i toplotna mapa (I) pokazuju značajno obogaćenje cJun.ROR1 ćelija u progenitorskim nišama.
(J, K) Reprezentativna protočna citometrija i kvantifikacija TCF1⁺TIM-3⁻ („stem-like“) podskupa unutar PD-1⁺ CAR-T populacije u tumoru. n = 3–4 miša/grupi.
(L) Direktno poređenje (koinfuzija) zastupljenosti „stem-like“ ćelija kod cJun.ROR1 (CD45.2⁺) i ROR1 (CD45.1⁺) varijanti u istom domaćinu 9. dana. n = 8 miševa.
Statistička analiza: (E) neupareni t-test, (K) dvofaktorska ANOVA (Sidakov test), (L) upareni t-test. Rezultati dva nezavisna eksperimenta.
*P < 0,05; **P < 0,01; ***P < 0,001; ****P < 0,0001.
Intratumorski rezervoar: „Baza“ na neočekivanom mestu
U klasičnoj imunologiji, pravila su jasna: TCF1⁺ progenitorske T ćelije se drže limfnih čvorova kao „sigurne kuće“. Tamo im dendritične ćelije pružaju neophodne MHC-zavisne signale za dugoročno održavanje i samorenovaciju.
Gde standardne CAR-T ćelije greše?
One jednostavno ne uspevaju da uspostave ovaj vitalni rezervoar u limfnim tkivima, prvenstveno zbog svog MHC-nezavisnog dizajna. Međutim, Snyder i saradnici su primenili precizan genetski inženjering kako bi premostili ovaj nedostatak. Rezultat? Modifikovane CAR-T ćelije formiraju PD-1⁺TCF1⁺ rezervoar direktno u tumorskom tkivu! Ovo je ključna funkcionalna adaptacija. Umesto oslanjanja na zaštitu u limfnim čvorovima, ove ćelije formiraju sopstvenu progenitorsku „tvrđavu“ unutar samog tumora. To im daje stratešku prednost: kontinuiranu produkciju novih efektorskih ćelija direktno na liniji fronta, tamo gde su najpotrebnije.
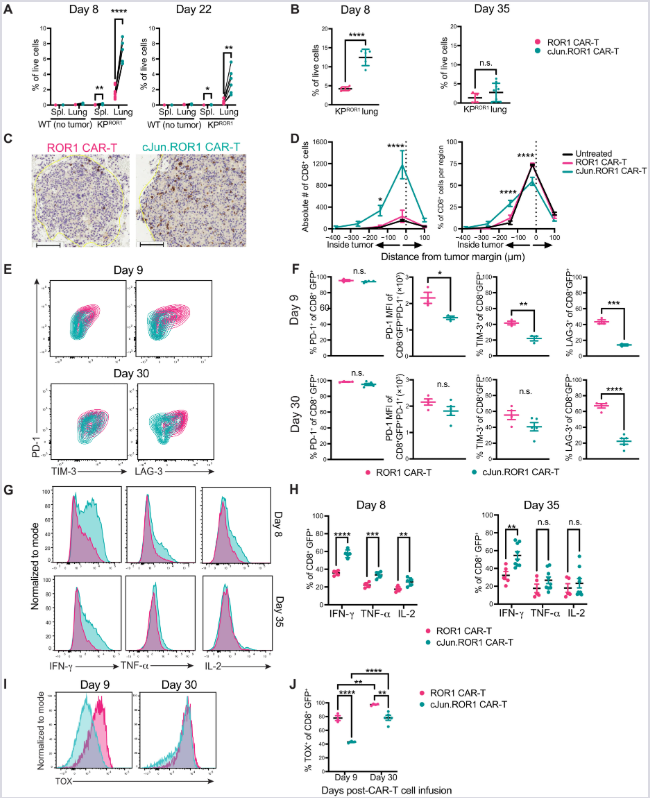
(A, B) Upoređivanje zastupljenosti cJun.ROR1 vs. ROR1 ćelija u slezini i plućima (koinfuzija vs. pojedinačna infuzija) kod WT i KPROR1 miševa (dan 8–35). n = 2–9 miševa po grupi.
(C, D) Imunohistohemijska (IHC) analiza CD8⁺ infiltracije u plućima 21. dana. Kvantifikacija (D) potvrđuje značajno veću gustinu cJun.ROR1 ćelija unutar granica tumora. Skala: 100 μm. n = 3 miša/grupi.
(E, F) Ekspresija inhibitornih receptora (PD-1, TIM-3, LAG-3) na CD8⁺ CAR-T ćelijama 9. i 30. dana. c-Jun značajno odlaže, ali ne sprečava iscrpljenost. n = 3–5 miševa/grupi.
(G, H) Intracelularna produkcija citokina (IFN-γ, TNF-α, IL-2) nakon ex vivo restimulacije (dan 8 i 35). c-Jun održava polifunkcionalnost ćelija tokom vremena. n = 5–9 miševa/grupi.
(I, J) Ekspresija transkripcionog faktora TOX (markera terminalne iscrpljenosti) u tumorima. n = 3–5 miševa/grupi.
Statistička analiza: (A) upareni t-test, (B, F, H) neupareni t-test, (D, J) dvofaktorska ANOVA (Tukey-jev test). Rezultati 2–5 nezavisnih eksperimenata.
*P < 0,05; **P < 0,01; ***P < 0,001; ****P < 0,0001.
c-Jun: Transkripcioni „telohranitelj“ za Tcf7 gen
Kada su autori odlučili da intervenišu, fokusirali su se na AP-1 porodicu transkripcionih faktora, konkretno na c-Jun i BATF. Iako oba pripadaju istoj porodici, rezultati su bili dijametralno suprotni.
Zašto je c-Jun ključan u ovoj studiji?
On deluje kao unutrašnji stabilizator koji sprečava epigenetsko gašenje progenitorskog programa:
- Smanjenje represivnih markera: c-Jun drastično redukuje nivoe H3K27me3 modifikacija na Tcf7 lokusu, efektivno držeći gen „otvorenim“.
- Održavanje fenotipa: Aktivno promoviše ekspresiju TCF1 i gura ćeliju ka progenitorskom i memorijskom profilu.
c-Jun ovde nastupa kao svojevrsni „bodyguard“ koji sprečava epigenetsko utišavanje Tcf7 gena. To omogućava CAR-T ćelijama da zadrže svoj „stem-like“ potencijal čak i u surovom mikrookruženju solidnog tumora.
Važna napomena: Specifičnost AP-1 faktora
Ovde imamo i kritičnu lekciju iz opreza: nisu svi AP-1 faktori saveznici. Povećana ekspresija BATF-a dovela je do potpuno drugačijeg scenarija. Umesto stabilizacije rezervoara, BATF je forsirao terminalnu diferencijaciju – ćelije su ubrzano sazrevale i još brže prelazile u stanje funkcionalne iscrpljenosti. U ovom kontekstu, c-Jun gradi unutrašnju „bazu“ za regeneraciju, dok BATF samo ubrzava put ka terminalnom otkazivanju.
Posttranskripciona sabotaža: Kako PD-1 receptori „tope“ c-Jun proteine?
PD-1 ne deluje samo kao transkripciona kočnica. On aktivno sabotira stabilnost samog c-Jun proteina. Aktivacija PD-1 receptora inhibira MAPK i PI3K signalne puteve, koji su u fiziološkim uslovima zaduženi za fosforilaciju i stabilizaciju c-Jun-a. Bez te podrške, c-Jun postaje nestabilan i podložan ubrzanoj proteozomskoj degradaciji – navode Snyder i saradnici.
PD-1 signalizacija destabilizuje c-Jun
„PD-1 ne deluje samo kao transkripciona kočnica. On aktivno sabotira stabilnost samog c-Jun proteina. Aktivacija PD-1 receptora inhibira MAPK i PI3K signalne puteve, koji su u fiziološkim uslovima zaduženi za fosforilaciju i stabilizaciju c-Jun-a. Bez te podrške, c-Jun postaje nestabilan i podložan ubrzanoj proteozomskoj degradaciji“ – navode Snyder i saradnici.
PD-1 ne menja samo gene; on aktivno smanjuje količinu c-Jun proteina unutar ćelije. Blokada PD-L1 puta ima suprotan efekat — ona ponovo pali MAPK/PI3K signalizaciju, čime „spasava“ c-Jun od uništenja.
Kombinacija c-Jun modifikacije i PD-L1 blokade: „The Perfect Storm“
Zanimljivo je da sama overekspresija c-Jun, iako značajno poboljšava fenotip ćelija, nije bila dovoljna za potpunu eliminaciju tumora. Pravi terapijski proboj nastaje tek u sinergiji sa anti-PD-L1 antitelima.
Ovaj pristup je doveo do dramatičnog, desetostrukog povećanja infiltracije CAR-T ćelija. Kod standardnih CAR-T ćelija, isti ovaj checkpoint inhibitor nije pokazao nikakav značajan efekat.
Ovde vidimo sinergiju u najčistijem obliku. Povećana ekspresija c-Jun-a stvara potencijal za rezervoar, ali blokada PD-L1 je neophodna da bi se taj potencijal realizovao. U agresivnim modelima NSCLC i TNBC, ova kombinacija je rezultovala skoro potpunom eliminacijom tumora — cilj koji je do sada bio nedostižan za klasičan CAR-T dizajn.
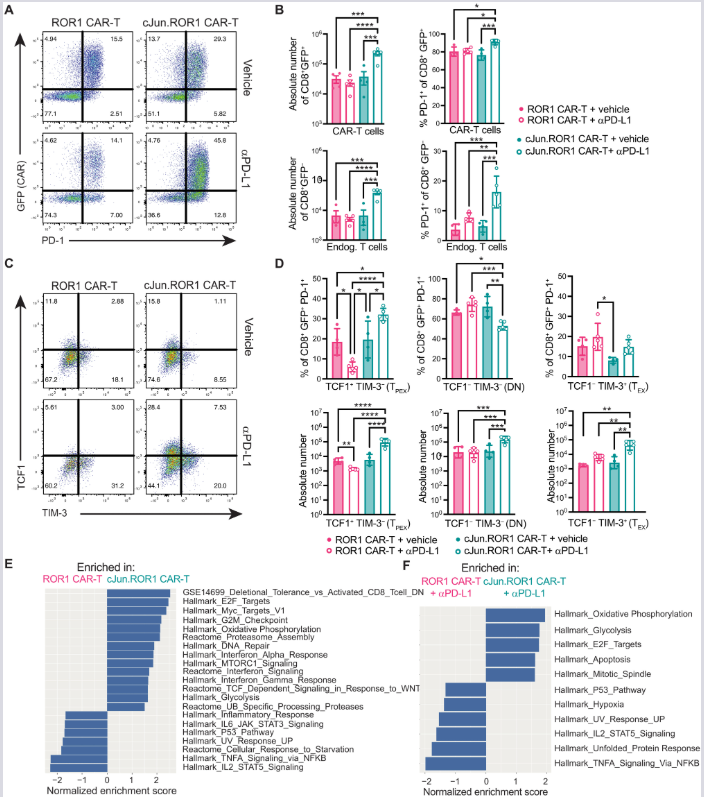
(A, B) Ekspresija PD-1 i apsolutni broj CD8⁺ CAR-T (GFP⁺) i endogenih (GFP⁻) T ćelija u plućima 5. dana nakon infuzije. n = 4–5 miševa/grupi. Kombinovana terapija dovodi do masovne akumulacije CAR-T ćelija.
(C, D) Reprezentativna protočna citometrija i kvantifikacija subpopulacija unutar PD-1⁺ CAR-T rezervoara:
TPEX (TCF1⁺TIM-3⁻ „stem-like“ progenitorske ćelije)
DN (TCF1⁻TIM-3⁻ dvostruko negativne ćelije)
TEX (TCF1⁻TIM-3⁺ terminalno iscrpljene ćelije)
n = 4–5 miševa/grupi.
(E, F) GSEA analiza (Normalized Enrichment Scores) za ROR1 vs. cJun.ROR1 ćelije tretirane vehikulumom (E) ili anti-PD-L1 antitelom (F). Rezultati potvrđuju superioran progenitorski profil c-Jun modifikovanih ćelija pod dejstvom checkpoint blokade. n = 3–5 miševa/grupi.
Statistička analiza: (B, D) jednofaktorska ANOVA (Holm–Šidák test). Rezultati dva nezavisna eksperimenta.
*P < 0,05; **P < 0,01; ***P < 0,001; ****P < 0,0001.
Sinergija sa endogenim T ćelijama: Više od direktne citotoksičnosti
Jedan od najintrigantnijih nalaza studije jeste da efekat nije ograničen samo na unete ćelije. U tumorskom mikrookruženju dokumentovano je regrutovanje i aktivacija endogenih CD8⁺ T ćelija domaćina. CAR-T terapija ovde prestaje da bude „usamljeni jahač“. Ona zapravo menja imunološki kontekst tumora („pretvara hladan tumor u topao“), mobilišući pacijentov sopstveni adaptivni imunitet da prepozna i napadne maligne ćelije.
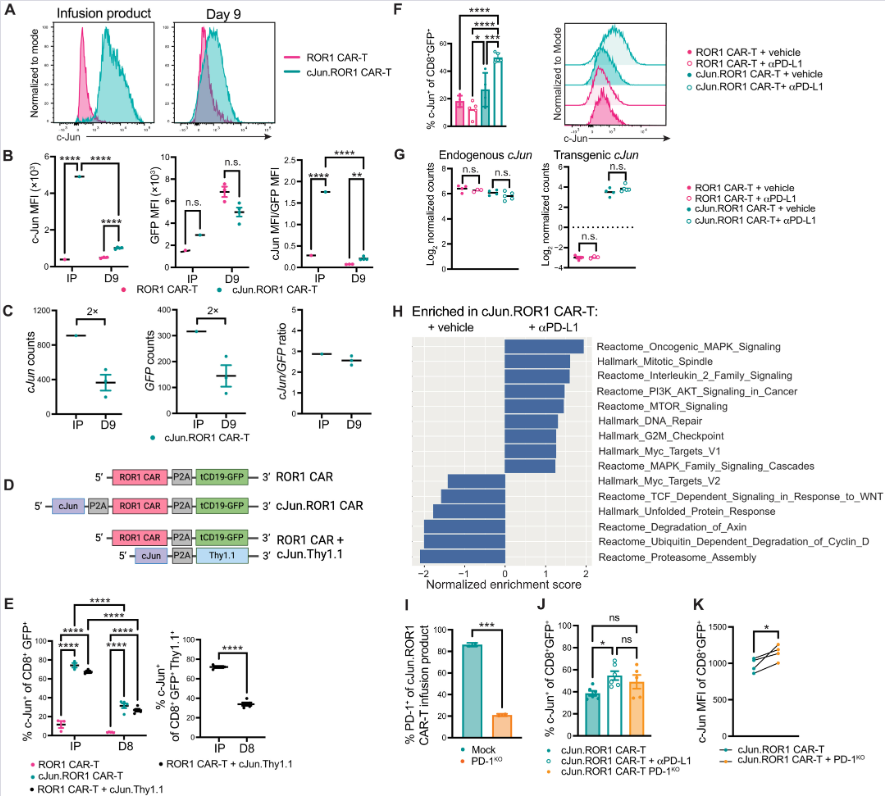
(A–C) Analiza nivoa c-Jun proteina (MFI) i mRNK (pseudobulk) u CAR-T ćelijama pre infuzije (IP) i u tumoru (dan 9). Uprkos stabilnoj transkripciji, nivo proteina u tumoru drastično opada. n = 3–4 miša/grupi.
(D–F) Šematski prikaz konstrukata i kvantifikacija c-Jun proteina u cJun.ROR1 ćelijama (dan 5 i 8). Blokada PD-L1 značajno povećava stabilnost c-Jun proteina u tumorskom mikrookruženju. n = 4–5 miševa/grupi.
(G, H) Log₂ normalizovana očitavanja i GSEA analiza obogaćenih genskih skupova u cJun.ROR1 ćelijama (dan 5). n = 3–5 miševa/grupi.
(I) CRISPR–Cas9 modifikacija PD-1 u CAR-T ćelijama potvrđuje direktnu ulogu ovog receptora u regulaciji nivoa c-Jun proteina nakon stimulacije.
(J, K) Nivo c-Jun proteina u metastatskim KPROR1 modelima 9. dana (infuzija vs. koinfuzija). n = 4–6 miševa/grupi.
Statistička analiza: (B) dvofaktorska ANOVA (Fisher-ov LSD), (C, E, I) neupareni t-test, (F, G, J) jednofaktorska ANOVA (Tukey-jev test), (K) upareni t-test. Rezultati dva nezavisna eksperimenta.
*P < 0,05; **P < 0,01; ***P < 0,001; ****P < 0,0001.
Zaključak
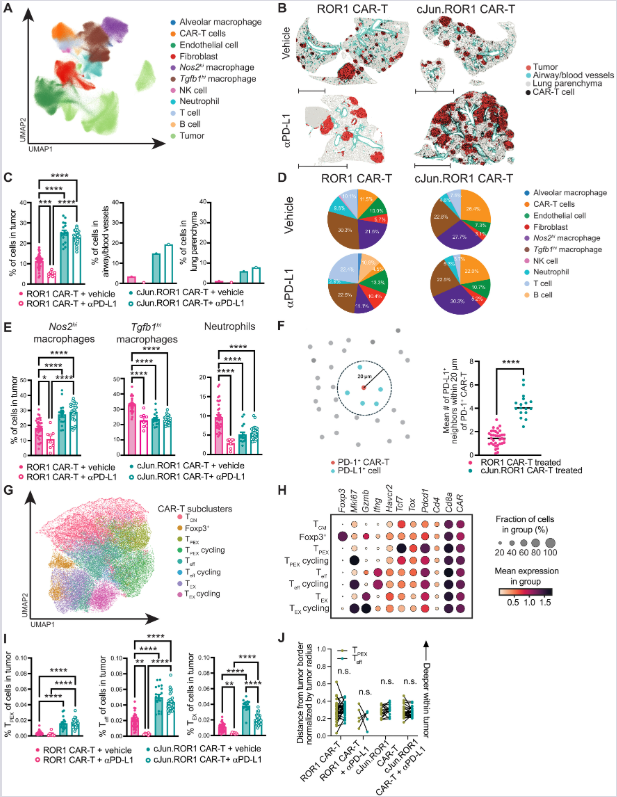
(A–D) Prostorna transkriptomika pluća KPROR1 miševa (dan 7). Klasterovanje (A) i vizuelni prikaz (B) identifikuju distribuciju CAR-T ćelija u tumorskim nodusima. Tortni dijagrami (D) potvrđuju promenu sastava infiltrata nakon terapije. n = 1 pluće po grupi.
(E, F) Analiza prostorne blizine (radijus 20 μm): cJun.ROR1 ćelije pokazuju značajno veću frekvenciju kontakta sa PD-L1⁺ mijeloidnim ćelijama u poređenju sa standardnim CAR-T ćelijama. n = 17–35 nodusa.
(G–I) Subklasterovanje CAR-T ćelija na osnovu prostorne ekspresije gena. Dot-plot (H) i kvantifikacija (I) potvrđuju da c-Jun modifikacija uz anti-PD-L1 dramatično smanjuje udeo terminalno diferenciranih ćelija u korist progenitorskih populacija. n = 6–35 nodusa.
(J) Analiza udaljenosti od granice tumora (normalizovana na radijus nodusa). Povezujuće linije potvrđuju očuvanje TPEX i Teff podskupova unutar samog tumora. n = 8–35 nodusa.
Statistička analiza: (C, E, I) jednofaktorska ANOVA (Tukey-jev test), (F) neupareni t-test, (J) upareni t-test.
*P < 0,05; **P < 0,01; ***P < 0,001; ****P < 0,0001.
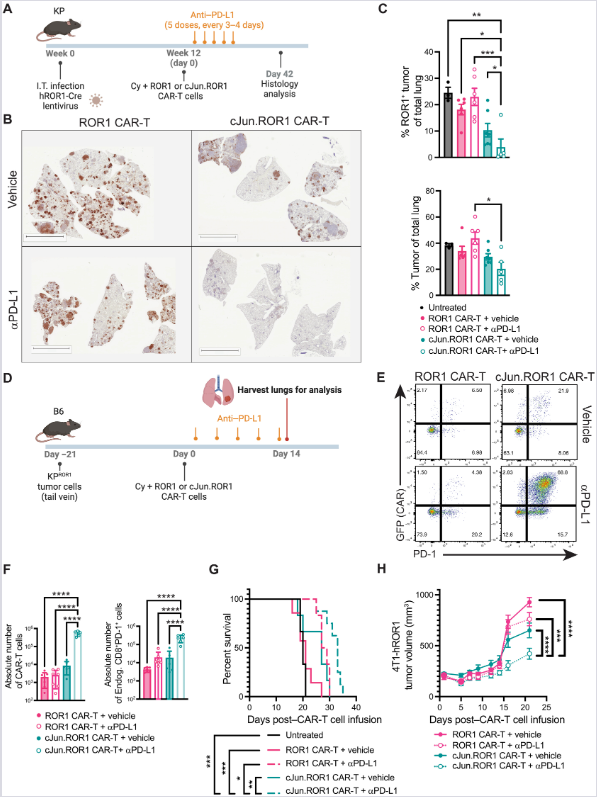
(A–C) Terapijski protokol i imunohistohemijska (IHC) analiza autohtonih KPROR1 tumora pluća (dan 42). Kvantifikacija ROR1⁺ tumorskih nodusa i ukupnog tumorskog opterećenja (C) potvrđuje superiornost kombinovane terapije (c-Jun + anti-PD-L1) u poređenju sa svim kontrolnim grupama. n = 3–7 miševa/grupi. Skala: 5 mm.
(D–F) Model metastatskih KP-ROR1 tumora. Protočna citometrija (E) i apsolutni broj CD8⁺ T ćelija (F) 14. dana pokazuju masovnu akumulaciju kako genetski modifikovanih CAR-T ćelija, tako i endogenih PD-1⁺ T ćelija domaćina pod dejstvom kombinovane terapije. n = 3–7 miševa/grupi.
(G) Krive preživljavanja (Kaplan-Meier) miševa sa transplantiranim KPROR1 tumorima. Kombinovani tretman dramatično produžava preživljavanje u poređenju sa standardnim CAR-T ćelijama. n = 3–8 miševa/grupi.
(H) Kinetika rasta tumora u ortotopskom modelu 4T1-ROR1 (karcinom dojke), koji dodatno potvrđuje univerzalnost ovog terapijskog pristupa kod različitih tipova solidnih tumora. n = 7–9 miševa/grupi.
Statistička analiza: (C, F) jednofaktorska ANOVA (Tukey-jev test), (G) log-rank Mantel–Cox test, (H) dvofaktorska ANOVA (Tukey-jev test). Rezultati dva nezavisna eksperimenta.
*P < 0,05; **P < 0,01; ***P < 0,001; ****P < 0,0001.
Rezultati ove studije redefinišu naše razumevanje rezistencije solidnih tumora. Glavna prepreka nije samo prodor u tumor, već epigenetski „lockdown“ i sledstveni gubitak vitalnog PD-1⁺TCF1⁺ rezervoara.
Modulacija c-Jun transkripcionog faktora nudi trostruko rešenje:
- Epigenetska zaštita: Direktno štiti Tcf7 gen od represivnog utišavanja.
- Intratumorska baza: Formira progenitorski rezervoar direktno u tumorskom tkivu za kontinuiranu obnovu efektorskih snaga.
- Senzitizacija na ICI: Programira CAR-T ćelije tako da postanu osetljive na standardnu checkpoint blokadu.
Ovo je snažan racional za novu generaciju imunoterapije koja kombinuje precizni ćelijski inženjering sa inhibitorima imunskih kontrolnih tačaka. Cilj je da CAR-T postane podjednako moćno oružje protiv solidnih maligniteta kao što je to već postala u hematologiji.
Referenca: Rad objavljen u Science Immunology možete pronaći ovde.
Tekst predstavlja informativni prikaz objavljene naučne literature. Ne sadrži kliničke preporuke i ne može zameniti stručnu procenu lekara u realnim okolnostima. Pericardion nema finansijski niti komercijalni interes povezan sa temom ili sadržajem ovog teksta.